
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
Il cloro isotopo con 18 neutroni ha un'abbondanza di 0,7577 e un numero di massa di 35 amu. Per calcolare il media massa atomica, moltiplicare la frazione per il numero di massa per ciascuna isotopo , quindi aggiungili insieme.
Allo stesso modo, qual è la media pesata di tutti gli isotopi di un elemento?
Usando le masse dei diversi isotopi e quanto abbondante ciascuno isotopo è, possiamo trovare il media massa degli atomi di an elemento . La massa atomica di an elemento è il media ponderata massa degli atomi in un campione naturale di elemento . La massa atomica è tipicamente riportata in unità di massa atomica.
cos'ha una massa di 1 amu? Un'unità di massa atomica (simboleggiata AMU o amu) è definita esattamente come 1/12 della massa di un atomo di carbonio-12. L'atomo di carbonio-12 (C-12) ha sei protoni e sei neutroni nel suo nucleo. In termini imprecisi, un AMU è la media dei protone massa a riposo e neutrone massa a riposo.
In secondo luogo, come si calcola l'abbondanza percentuale utilizzando la massa atomica?
Cambia ciascuno percentuale di abbondanza in forma decimale dividendo per 100. Moltiplica questo valore per massa atomica di quell'isotopo. Somma per ogni isotopo per ottenere la media massa atomica.
Qual è la differenza tra massa atomica e peso atomico?
Massa atomica (mun) è il messa di un atomo . Una sola atomo ha un determinato numero di protoni e neutroni, quindi il messa è inequivocabile (non cambierà) ed è la somma del numero di protoni e neutroni nell'atomo . Peso atomico è una media ponderata di messa di tutti i atomi di un elemento, in base all'abbondanza di isotopi.
Consigliato:
Come si trova la velocità media con due velocità?
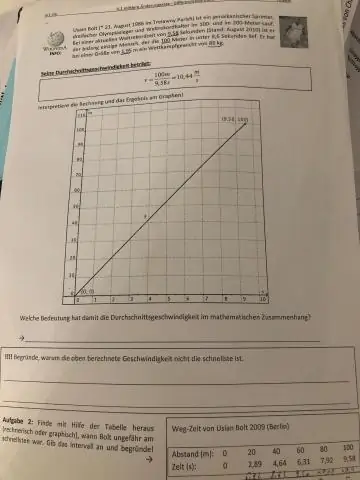
La somma della velocità iniziale e finale è divisa per 2 per trovare la media. Il calcolatore della velocità media utilizza la formula che mostra che la velocità media (v) è uguale alla somma della velocità finale (v) e della velocità iniziale (u), divisa per 2
Come si trova la proporzione media?
Il modo per trovare una media proporzionale è moltiplicare i due numeri insieme, quindi trovare la loro radice quadrata. Questa sarà la media proporzionale
Come si trova il calcolo della velocità media?

(b) La velocità media è la pendenza della linea secante, piuttosto che la pendenza della linea tangente. Trovare la velocità media è facile. Sostituisci t = 2 et = 3 nell'equazione di posizione per calcolare l'altezza dell'oggetto ai confini dell'intervallo indicato per generare due coppie ordinate: (2, 1478) e (3, 1398)
Come si trova la media su un grafico?
Per trovare la media, aggiungi i numeri e dividi la somma per il numero di addendi
Come si trova il valore atteso della media campionaria?

Il valore atteso della media campionaria è la media della popolazione e l'SE della media campionaria è la DS della popolazione, divisa per la radice quadrata della dimensione del campione
