
Sommario:
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
Nel numero di ossidazione metodo, si determina il numeri di ossidazione di tutti gli atomi. Poi moltiplichi gli atomi che sono cambiati per piccoli interi numeri . Stai rendendo la perdita totale di elettroni uguale al guadagno totale di elettroni. Allora lei bilancia il resto degli atomi.
Di conseguenza, come bilanciare le equazioni di riduzione dell'ossidazione?
Segui queste regole per bilanciare semplici equazioni redox:
- Scrivi le semireazioni di ossidazione e riduzione per la specie che viene ridotta o ossidata.
- Moltiplica le semireazioni per il numero appropriato in modo che abbiano lo stesso numero di elettroni.
- Aggiungi le due equazioni per eliminare gli elettroni.
In secondo luogo, come si bilanciano le equazioni? Metodo 1 Fare un Equilibrio Tradizionale
- Scrivi la tua equazione data.
- Scrivi il numero di atomi per elemento.
- Risparmia l'idrogeno e l'ossigeno per ultimi, poiché spesso sono su entrambi i lati.
- Inizia con singoli elementi.
- Usa un coefficiente per bilanciare il singolo atomo di carbonio.
- Bilancia poi gli atomi di idrogeno.
- Bilancia gli atomi di ossigeno.
Inoltre, come si bilanciano facilmente le equazioni chimiche?
In generale, per bilanciare un'equazione, ecco le cose che dobbiamo fare:
- Contare gli atomi di ciascun elemento nei reagenti e nei prodotti.
- Usa coefficienti; posizionarli davanti ai composti secondo necessità.
C o2 co2 è una reazione redox?
È c + O2 = CO2 un intramolecolare reazione redox o no? Un reagente (carbonio) viene ossidato e l'altro (ossigeno) viene ridotto. Quindi questo è un semplice intermolecolare reazione redox . Qualunque reazione in cui uno o più reagenti/prodotti sono elementi puri devono essere a reazione redox.
Consigliato:
Quali tipi di numeri costituiscono l'insieme dei numeri chiamati numeri reali?

Insiemi di numeri reali (interi positivi) o i numeri interi {0, 1, 2, 3,} (interi non negativi). I matematici usano il termine "naturale" in entrambi i casi
Cosa sono i numeri naturali i numeri interi e i numeri razionali?
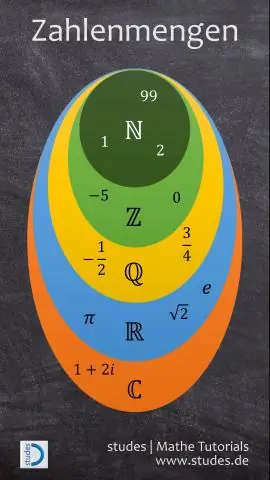
I numeri reali sono principalmente classificati in numeri razionali e irrazionali. I numeri razionali includono tutti gli interi e le frazioni. Tutti gli interi negativi e i numeri interi costituiscono l'insieme degli interi. I numeri interi comprendono tutti i numeri naturali e zero
Come si risolvono i numeri complessi e i numeri immaginari?

I numeri complessi hanno la forma a+bi a + b i, dove aeb sono numeri reali e i è la radice quadrata di −1. Tutti i numeri reali possono essere scritti come numeri complessi impostando b=0. I numeri immaginari hanno la forma bi e possono essere scritti anche come numeri complessi ponendo a=0
Come si bilanciano gli esempi di equazioni chimiche?

Esempi di 10 equazioni chimiche bilanciate Scrivere equazioni chimiche bilanciate è essenziale per le lezioni di chimica. 6 CO2 + 6 H2O → C6H12O6 + 6 O2 (equazione bilanciata per la fotosintesi) 2 AgI + Na2S → Ag2S + 2 NaI. Ba3N2 + 6 H2O → 3 Ba(OH)2 + 2 NH3 3 CaCl2 + 2 Na3PO4 → Ca3(PO4)2 + 6 NaCl. 4 FeS + 7 O2 → 2 Fe2O3 + 4 SO2
Come bilanciare le seguenti equazioni?

VIDEO Rispetto a questo, come si bilancia un'equazione chimica? Per bilancia un equazione chimica , inizia scrivendo il numero di atomi in ciascun elemento, che è elencato nel pedice accanto a ciascun atomo. Quindi, aggiungi coefficienti agli atomi su ciascun lato del equazione a bilancia loro con gli stessi atomi dall'altra parte.
