
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
In zero - cinetica dell'ordine , il Vota di una reazione non non dipendono dalla concentrazione del substrato. il t 1 /2 formula per una reazione di ordine zero suggerisce il metà - vita dipende dalla quantità di concentrazione iniziale e tasso costante.
Successivamente, ci si potrebbe anche chiedere, qual è l'emivita per una reazione di ordine zero?
96 secondi
Inoltre, come si trova l'emivita di una costante di velocità? Strategia:
- Utilizzare l'equazione 3 per calcolare l'emivita della reazione.
- Moltiplicare la concentrazione iniziale per 1/2 alla potenza corrispondente al numero di emivite per ottenere le concentrazioni rimanenti dopo quelle emivite.
- Sottrarre la concentrazione rimanente dalla concentrazione iniziale.
A questo proposito, perché l'emivita di una reazione del primo ordine è costante?
In altre parole, la concentrazione iniziale del reagente non ha alcuna influenza sulla metà - vita del reazione , cioè il metà - vita è costante indipendentemente dalla concentrazione del reagente.
L'emivita di una reazione di ordine zero dipende dalla concentrazione iniziale del reagente?
Quindi, dall'equazione di cui sopra Potere concludere che il l'emivita di una reazione di ordine zero dipende Su concentrazione iniziale di specie reagenti e la costante di velocità, k. è direttamente proporzionale a concentrazione iniziale del reagente mentre è inversamente proporzionale alla costante di velocità, k.
Consigliato:
In che modo la struttura del cloroplasto è correlata alla sua funzione?
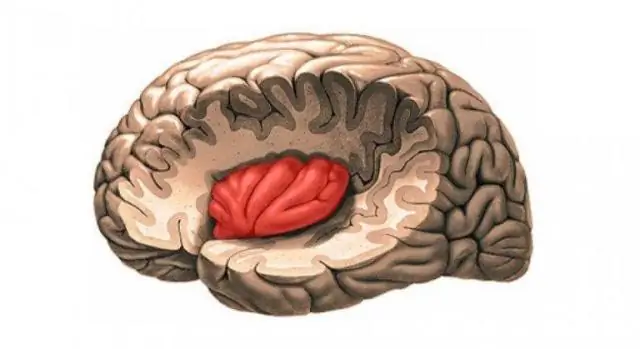
Cloroplasto. La struttura del cloroplasto è adattata alla funzione che svolge: Tilacoidi: i dischi appiattiti hanno un piccolo volume interno per massimizzare il gradiente di idrogeno all'accumulo di protoni. Fotosistemi – pigmenti organizzati in fotosistemi nella membrana tilacoide per massimizzare l'assorbimento della luce
Qual è l'emivita di una reazione di ordine zero?

L'emivita di una reazione è il tempo necessario per diminuire della metà la quantità di un determinato reagente. L'emivita di una reazione di ordine zero diminuisce al diminuire della concentrazione iniziale del reagente nella reazione
Quali sono le unità di velocità costante per la reazione del primo ordine?

Nelle reazioni del primo ordine, la velocità di reazione è direttamente proporzionale alla concentrazione del reagente e le unità delle costanti di velocità del primo ordine sono 1/sec. Nelle reazioni bimolecolari con due reagenti, le costanti di velocità del secondo ordine hanno unità di1/M*sec
In che modo il prodotto prodotto al minuto potrebbe essere correlato alla velocità di una reazione catalizzata da un enzima?
Per una reazione catalizzata da enzimi, la velocità è solitamente espressa nella quantità di prodotto prodotto al minuto. A bassa temperatura, il riscaldamento di solito aumenta la velocità di una reazione catalizzata da enzimi perché i reagenti hanno più energia e possono raggiungere più facilmente il livello di energia di attivazione
In che modo la lunghezza d'onda è correlata alla velocità della luce in un mezzo?

La velocità della luce in un mezzo è v=cn v = c n, dove n è il suo indice di rifrazione. Ciò implica che v = fλn, dove λn è la lunghezza d'onda in un mezzo e che λn=λn λ n = λ n, dove λ è la lunghezza d'onda nel vuoto e n è l'indice di rifrazione del mezzo
