
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
La neutralizzazione comporta un reazione acida insieme a una base o an alcali , formando un sale e acqua.
Allo stesso modo ci si potrebbe chiedere, che tipo di reazione è l'acido alcalino?
Una reazione acido-alcali è un caso speciale di una reazione acido-base, in cui anche la base utilizzata è un alcali. Quando un acido reagisce con un sale alcalino (un idrossido metallico), il prodotto è un sale metallico e acqua . Le reazioni acido-alcali sono anche reazioni di neutralizzazione.
Allo stesso modo, cos'è una reazione di neutralizzazione? UN reazione di neutralizzazione è quando un acido e una base reagire per formare acqua e un sale e prevede la combinazione di H+ ioni e OH- ioni per generare acqua. Il neutralizzazione di un acido forte e una base forte ha un pH pari a 7. Tabella 1: Gli acidi e le basi forti più comuni.
Le persone chiedono anche, cosa succede al pH durante una reazione di neutralizzazione?
Neutralizzazione è il reazione di un acido con una base che risulta nella pH andando verso 7. È un processo utile che si verifica nella vita di tutti i giorni come nel trattamento dell'indigestione acida e nel trattamento del terreno acido con l'aggiunta di calce. Neutralizzazione muove anche il pH di un alcali verso il sette.
Quali sostanze possono reagire con un acido per formare un sale solubile?
Metallo Gli ossidi possono anche essere usati come basi ed essere fatti reagire con acidi per produrre sali e acqua. Mentre abbastanza reattivo metalli può essere fatto reagire con acidi per formare sale e idrogeno, sali di molto non reattivi metalli , come il rame, non può essere fatto in questo modo perché questi metalli non reagiscono con gli acidi.
Consigliato:
Come si chiama il processo di produzione dell'RNA dal DNA?
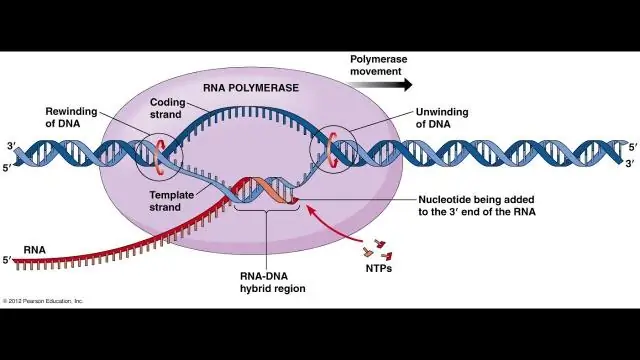
Il processo di trasformazione del DNA in RNA per essere sintetizzato in proteine cellulari è chiamato trascrizione del DNA. La trascrizione è il primo passo per creare proteine all'interno delle cellule
Come neutralizzare un acido e un alcali?

Quando un acido reagisce con un alcali produce un sale e acqua. Questa reazione è chiamata neutralizzazione. L'alcali ha neutralizzato l'acido rimuovendo i suoi ioni H+ e trasformandoli in acqua
Come si chiama il processo che crea nuovi fondali oceanici da placche divergenti?

La diffusione del fondale marino è un processo che si verifica sulle dorsali oceaniche, dove si forma nuova crosta oceanica attraverso l'attività vulcanica e poi si allontana gradualmente dalla cresta
Cosa succede al pH Quando un acido viene aggiunto a un alcali?

L'aggiunta di acqua a un acido o una base ne cambierà il pH. L'acido sta diventando meno acido. Allo stesso modo, quando un alcali viene diluito con acqua, la concentrazione di ioni OH diminuisce. Ciò fa sì che il pH dell'alcali scenda verso 7, rendendo la soluzione meno alcalina man mano che viene aggiunta più acqua
Come si chiama la reazione quando un acido reagisce con una base?

La reazione di un acido con una base è detta reazione di neutralizzazione. I prodotti di questa reazione sono un sale e acqua. Ad esempio, la reazione di acido cloridrico, HCl, con soluzioni di idrossido di sodio, NaOH, produce una soluzione di cloruro di sodio, NaCl e alcune molecole d'acqua aggiuntive
