
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
Il molecolarità di una reazione è il numero di molecole che reagiscono in un elemento elementare fare un passo . Una reazione unimolecolare è quella in cui solo una molecola che reagisce partecipa alla reazione. Due molecole reagenti si scontrano tra loro in una reazione bimolecolare.
Considerando questo, qual è la Molecolarità di ciascuna reazione?
Il molecolarità per un reazione è definito per ogni passo individuale nel meccanismo del reazione . È uguale al numero di molecole partecipanti (o reagire ) in ogni passo elementare nel meccanismo della reazione.
In secondo luogo, quali sono la Molecolarità e la legge della velocità per ogni passaggio? Il molecolarità delle elementari fare un passo , e i reagenti coinvolti, determineranno quale sia il legge sui tassi sarà per quel particolare fare un passo nel meccanismo. Molecolarità delle elementari passi e corrispondente leggi sui tassi : Il molecolarità di un elementare fare un passo in un meccanismo di reazione determina la forma del suo legge sui tassi.
Inoltre, come si determina la Molecolarità?
Generalmente, molecolarità di semplici reazioni è uguale alla somma del numero di molecole di reagenti coinvolte nell'equazione stechiometrica bilanciata. Il molecolarità di una reazione è il numero di molecole reagenti che prendono parte a una singola fase della reazione.
Che cos'è un passaggio unimolecolare?
Passaggi unimolecolari sono passi che coinvolgono un solo reagente, passaggi bimolecolari coinvolgono 2 reagenti. Se la passi sono elementari passi in un meccanismo, il molecolarità è anche l'ordine di reazione per la velocità. Cioè un unimolecolare elementare fare un passo ha un tasso di primo ordine. 2.
Consigliato:
Che cos'è un passaggio elementare in un meccanismo di reazione?

Una fase elementare (o reazione elementare) è una fase di una serie di semplici reazioni che mostrano l'andamento di una reazione a livello molecolare. Un meccanismo di reazione è la sequenza di passaggi elementari che insieme compongono un'intera reazione chimica
Cos'è il passaggio seguito dal magma?

Condotto: un passaggio seguito dal magma in un vulcano. Cratere: una depressione dai lati ripidi, solitamente circolare, formata da un'esplosione o da un collasso in corrispondenza di una bocca vulcanica
Perché la trascrizione è un passaggio necessario nella sintesi proteica?
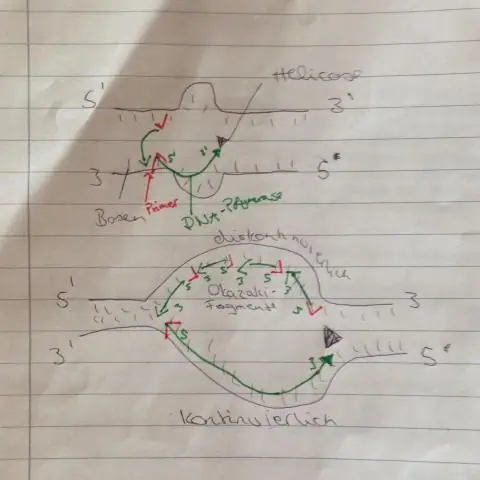
L'arte della sintesi proteica Nelle cellule eucariotiche, la trascrizione avviene nel nucleo. Durante la trascrizione, il DNA viene utilizzato come stampo per creare una molecola di RNA messaggero (mRNA). Durante la traduzione, il codice genetico nell'mRNA viene letto e utilizzato per produrre una proteina
Come si determina qual è il passaggio che determina la velocità?

La fase di determinazione della velocità è la fase più lenta di una reazione chimica che determina la velocità (velocità) alla quale procede la reazione complessiva. Risposta Il passo che determina la velocità è il secondo passo perché è il passo lento. 2NO+2H2→N2+2H2O. Gli intermedi in questa reazione sono N2O2 e N2O
Cos'è la Molecolarità di una reazione?

Molecolarità. La molecolarità di una reazione è definita come il numero di molecole o ioni che partecipano alla fase di determinazione della velocità. Un meccanismo in cui due specie reagenti si combinano nello stato di transizione della fase determinante la velocità è chiamato bimolecolare
