
- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
Possono essere trovati in diversi funzionali gruppi , come aldeidi, chetoni, esteri e molti altri. UN gruppo carbonilico può aumentare il punto di fusione o di ebollizione di un composto. È descritto come polare e reattivo e le cariche negative e positive su a carbonile contribuiscono alla polarità.
Di conseguenza, cosa fa il gruppo carbonilico?
All'interno della biologia, a gruppo carbonilico all'interno di una molecola le permette di subire le numerose reazioni necessarie per mantenere la vita. Molte comuni molecole biologiche contengono a gruppo carbonilico , che consente alla cellula la capacità di creare nuove molecole e modificare la molecola con una serie di altri funzionali gruppi.
Oltre sopra, come si forma il gruppo carbonilico? Negli acidi carbossilici e nei loro derivati, il gruppo carbonilico è attaccato a uno degli atomi di alogeno o a gruppi contenenti atomi come ossigeno, azoto o zolfo. Questi atomi influenzano la gruppo carbonilico , formando un nuovo funzionale gruppo con proprietà distintive.
Inoltre, qual è la natura del gruppo carbonilico?
UN gruppo carbonilico è un funzionale chimicamente organico gruppo composto da un atomo di carbonio doppiamente legato ad un atomo di ossigeno [C=O] Il più semplice gruppi carbonilici sono aldeidi e chetoni solitamente attaccati ad un altro composto di carbonio. Queste strutture possono essere trovate in molti aromatic composti contribuendo all'olfatto e al gusto.
Perché il gruppo carbonile è reattivo?
A causa della maggiore elettronegatività dell'ossigeno, il gruppo carbonilico è polare e le aldeidi e i chetoni hanno momenti di dipolo molecolare (D) più grandi degli alcheni. La polarità del gruppo carbonilico ha anche un profondo effetto sulla sua sostanza chimica reattività , rispetto ai doppi legami non polari degli alcheni.
Consigliato:
Perché l'idrogeno non fa parte di nessun gruppo?

Configurazione elettronica: 1s
Che cos'è in generale un gruppo funzionale e perché tali gruppi sono così importanti?

I gruppi funzionali sono attaccati allo scheletro carbonioso delle molecole organiche. Determinano le caratteristiche e la reattività chimica delle molecole. I gruppi funzionali sono molto meno stabili della spina dorsale del carbonio ed è probabile che partecipino alle reazioni chimiche
In che modo Avery e il suo gruppo hanno determinato quale molecola fosse più importante per la trasformazione?
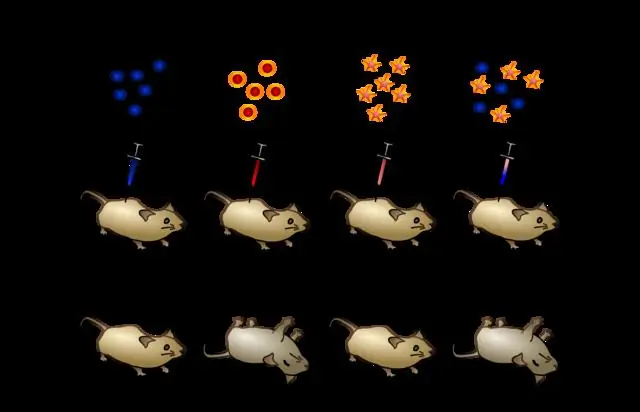
Descrivi brevemente come Avery e il suo gruppo hanno determinato quale molecola era più importante per la trasformazione. Avery e il suo gruppo hanno utilizzato due diversi enzimi su un estratto di batteri uccisi dal calore. Uno ha distrutto il DNA, l'altro ha distrutto tutto ma. Hanno scoperto che la trasformazione avveniva ancora quando era presente il DNA
Come si forma il gruppo carbonilico?

Negli acidi carbossilici e nei loro derivati, il gruppo carbonilico è legato a uno degli atomi di alogeno oa gruppi contenenti atomi come ossigeno, azoto o zolfo. Questi atomi influenzano il gruppo carbonilico, formando un nuovo gruppo funzionale con proprietà distintive
Quale gruppo funzionale è più importante per l'energia cellulare?

Con quattro atomi di ossigeno elettronegativi, i gruppi fosfato sono altamente reattivi e il trasferimento di un gruppo fosfato da una molecola all'altra fornisce energia alle reazioni chimiche. L'ATP, il principale vettore energetico nelle cellule, è composto da tre gruppi fosfato legati in successione
