- Autore Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Ultima modifica 2025-01-22 17:02.
Modello atomico di Bohr : Nel 1913 bohr proposto il suo guscio quantizzato modello del atomo a spiegare come elettroni può avere orbite stabili attorno al nucleo. L'energia di an elettrone dipende dalla dimensione dell'orbita ed è inferiore per orbite più piccole. La radiazione può verificarsi solo quando il elettrone salta da un'orbita all'altra.
Inoltre, come descrive Niels Bohr gli elettroni nel suo modello atomico?
orbitano attorno al nucleo centrale in percorsi discreti. elettroni orbitano attorno al nucleo in percorsi specifici e definiti. Ogni percorso ha un'energia specificata.
Inoltre, come trovò Bohr la sua teoria? Modello atomico The bohr Il modello mostra l'atomo come un piccolo nucleo carico positivamente circondato da elettroni orbitanti. bohr è stato il primo a scoprire che gli elettroni viaggiano in orbite separate attorno al nucleo e che il numero di elettroni nell'orbita esterna determina le proprietà di un elemento.
Allo stesso modo, cosa spiega il modello di Bohr?
Il Modello di Bohr mostra che gli elettroni negli atomi sono in orbite di energia diversa attorno al nucleo (si pensi ai pianeti che orbitano intorno al sole). bohr usava il termine livelli energetici (o gusci) per descrivere queste orbite di diversa energia.
In che modo Bohr si espanse sul modello dell'atomo di Rutherford?
bohr migliorato Il modello di Rutherford proponendo che gli elettroni viaggiassero attorno al nucleo in orbite che avevano specifici livelli di energia. Quando un metallo atomo viene riscaldato, assorbe energia e gli elettroni saltano a livelli energetici più elevati.
Consigliato:
In che modo gli spettri di emissione sono la prova dei gusci di elettroni nel modello di Bohr?

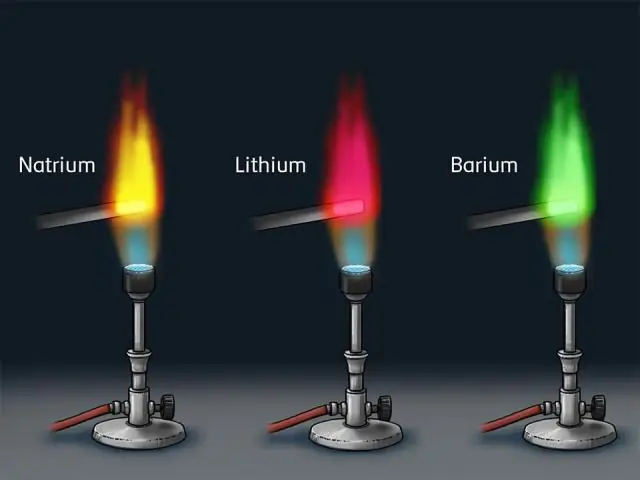
La presenza di solo determinate righe negli spettri atomici significava che un elettrone può adottare solo determinati livelli energetici discreti (l'energia è quantizzata); da qui l'idea dei gusci quantistici. Le frequenze dei fotoni assorbite o emesse da un atomo sono fissate dalle differenze tra i livelli energetici delle orbite
In che modo Bohr ha migliorato il modello atomico di Rutherford?

Bohr migliorò il modello atomico di Rutherford proponendo che gli elettroni viaggiassero in orbite circolari con specifici livelli di energia. Spiegazione: Rutherford propose che gli elettroni circondassero il nucleo come i pianeti intorno al sole. Quando un atomo di metallo viene riscaldato, assorbe energia e gli elettroni saltano a livelli di energia più elevati
In che modo Bohr ha scoperto il suo modello?

Nel 1913 Bohr propose il suo modello a guscio quantizzato dell'atomo per spiegare come gli elettroni possano avere orbite stabili attorno al nucleo. Per rimediare al problema della stabilità, Bohr modificò il modello di Rutherford richiedendo che gli elettroni si muovessero in orbite di dimensione ed energia fisse
Quale modello atomico afferma che è impossibile conoscere l'esatta posizione degli elettroni attorno al nucleo?

La risposta è il modello della nuvola elettronica. Il modello di Erwin Schrodinger, a differenza degli altri modelli, mostra gli elettroni come parte di una "nuvola" in cui tutti gli elettroni occupano lo stesso spazio contemporaneamente
In che modo Niels Bohr ha scoperto il modello planetario?

Modello atomico di Bohr: Nel 1913 Bohr propose il suo modello a guscio quantizzato dell'atomo per spiegare come gli elettroni possono avere orbite stabili attorno al nucleo. L'energia di un elettrone dipende dalla dimensione dell'orbita ed è inferiore per orbite più piccole. La radiazione può verificarsi solo quando l'elettrone salta da un'orbita all'altra
